上海中科新生命生物科技有限公司
18 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0
- 1
- 0
- 3
文献支持
G350肠道高通量靶向代谢组
询价
公司新闻/正文
Cell Metab | 烧烤太咸升血压?莫怕!江南大学揭示"降压卫士"植物乳杆菌靶向肠道微生物的作用机制
391 人阅读发布时间:2025-06-11 09:56
 高血压通常是由遗传因素和环境影响之间的相互作用引起的,其中高盐摄入是影响血压(BP)的重要环境因素,然而其诱导高血压的具体病理机制尚未完全阐明。迄今为止,大多数抗高血压药物都有不同程度的副作用,因此需要通过开发新的干预措施来解决人群的血压控制需求。
2025年2月,江南大学马鑫教授联合陈卫院士团队、翟齐啸教授团队在Cell Metabolism上发表名为“Targeting gut S. aureofaciensTü117 serves as a new potential therapeutic intervention for the prevention and treatment of hypertension”的研究文章,发现肠道微生物S. aureofaciens Tü117产生的α-脂霉素在高盐饮食(HSD)小鼠及原发性高血压患者中上调。α-脂霉素可靶向TRPV4,抑制钙离子内流,进而引起血管舒张障碍。补充植物乳杆菌CCFM639可降低前期或1期高血压且未服用抗高血压药物受试者的血压。
高血压通常是由遗传因素和环境影响之间的相互作用引起的,其中高盐摄入是影响血压(BP)的重要环境因素,然而其诱导高血压的具体病理机制尚未完全阐明。迄今为止,大多数抗高血压药物都有不同程度的副作用,因此需要通过开发新的干预措施来解决人群的血压控制需求。
2025年2月,江南大学马鑫教授联合陈卫院士团队、翟齐啸教授团队在Cell Metabolism上发表名为“Targeting gut S. aureofaciensTü117 serves as a new potential therapeutic intervention for the prevention and treatment of hypertension”的研究文章,发现肠道微生物S. aureofaciens Tü117产生的α-脂霉素在高盐饮食(HSD)小鼠及原发性高血压患者中上调。α-脂霉素可靶向TRPV4,抑制钙离子内流,进而引起血管舒张障碍。补充植物乳杆菌CCFM639可降低前期或1期高血压且未服用抗高血压药物受试者的血压。

研究材料
健康人群及原发性高血压患者的尿液、血清及粪便;C57BL/6J小鼠的血清、粪便及原代细胞
技术路线
步骤1:分析与高盐饮食相关的小分子代谢物
步骤2:证明肠道微生物S. aureofaciens Tü117与HSD相关高血压的关系
步骤3:挖掘S. aureofaciens Tü117相关α-脂霉素诱发高血压的分子机制
步骤4:探索植物乳杆菌的临床降压作用
研究结果
1. α-脂霉素是HSD相关高血压的关键代谢物
使用代谢组学分析了对照组和HSD小鼠的血清,发现由S. aureofaciens Tü117产生的α-脂霉素是HSD小鼠中最显着的特异性上调代谢物之一,表明循环α-脂霉素与HSD之间存在关联。此外,HSD小鼠的粪便 α-脂霉素含量也增加。静脉注射或灌肠给药α-脂霉素均可增加血压,因此作者假设,慢性HSD会改变肠道菌群群落,导致α-脂霉素水平升高。
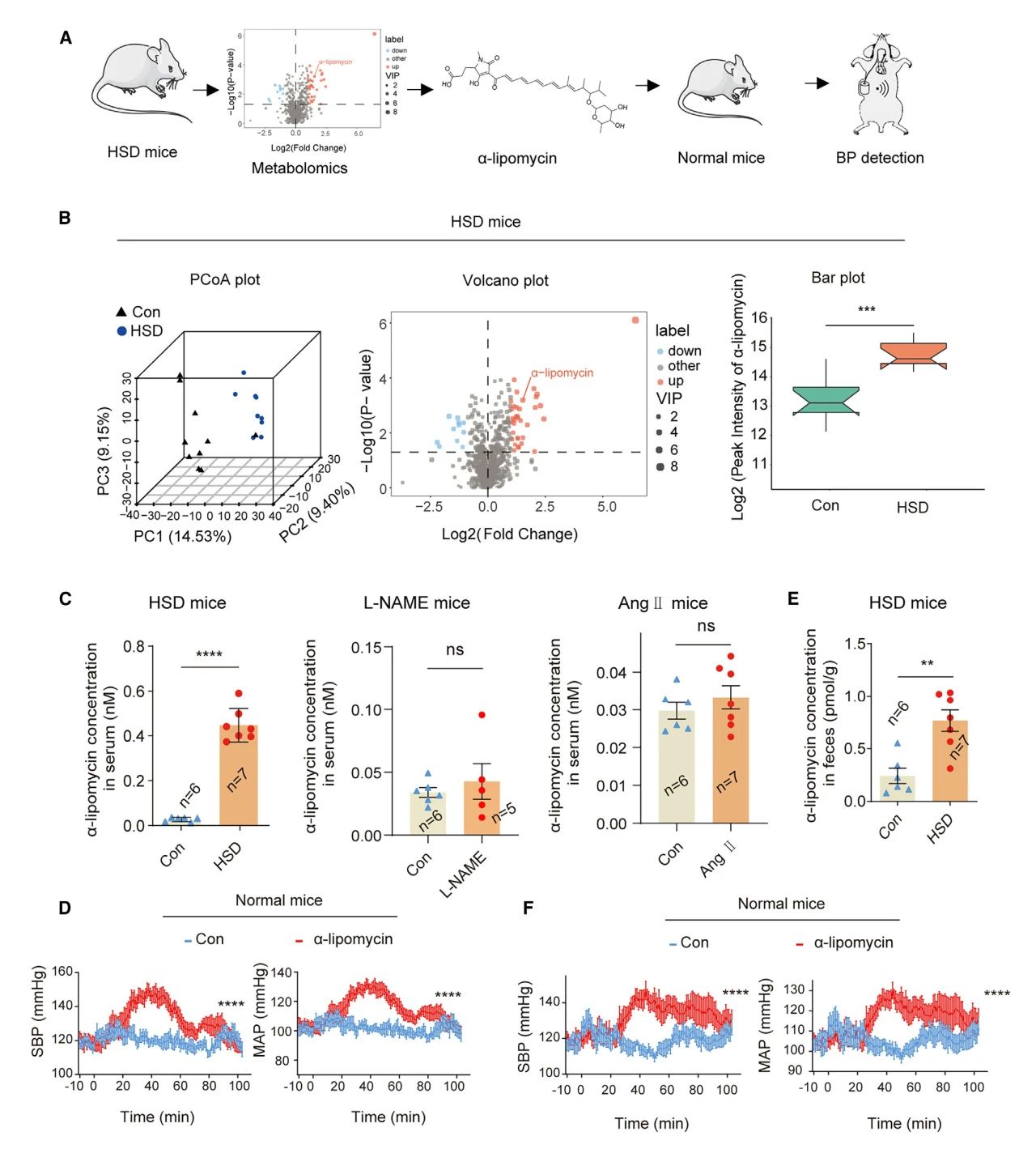 图1 α-脂霉素是与HSD相关高血压的关键代谢物
2. S. aureofaciens Tü117与HSD相关高血压有关
通过LC-MS分析,作者仅在S. aureofaciens Tü117的发酵液中检测到了α-脂霉素。此外,能够调节α-脂霉素表达的LipReg4基因也仅存在于S. aureofaciens Tü117中,且其mRNA水平在HSD小鼠的粪便及结肠中增加。这些结果表明S. aureofaciens Tü117与盐敏感高血压之间存在关联。
使用S. aureofaciens Tü117处理无菌鼠,增加了血清的α-脂霉素水平及小鼠血压,且α-脂霉素水平的显着变化发生在血压变化之前。表明S. aureofaciens Tü117-α-脂霉素轴的激活是盐敏感高血压进展的主要原因。
图1 α-脂霉素是与HSD相关高血压的关键代谢物
2. S. aureofaciens Tü117与HSD相关高血压有关
通过LC-MS分析,作者仅在S. aureofaciens Tü117的发酵液中检测到了α-脂霉素。此外,能够调节α-脂霉素表达的LipReg4基因也仅存在于S. aureofaciens Tü117中,且其mRNA水平在HSD小鼠的粪便及结肠中增加。这些结果表明S. aureofaciens Tü117与盐敏感高血压之间存在关联。
使用S. aureofaciens Tü117处理无菌鼠,增加了血清的α-脂霉素水平及小鼠血压,且α-脂霉素水平的显着变化发生在血压变化之前。表明S. aureofaciens Tü117-α-脂霉素轴的激活是盐敏感高血压进展的主要原因。
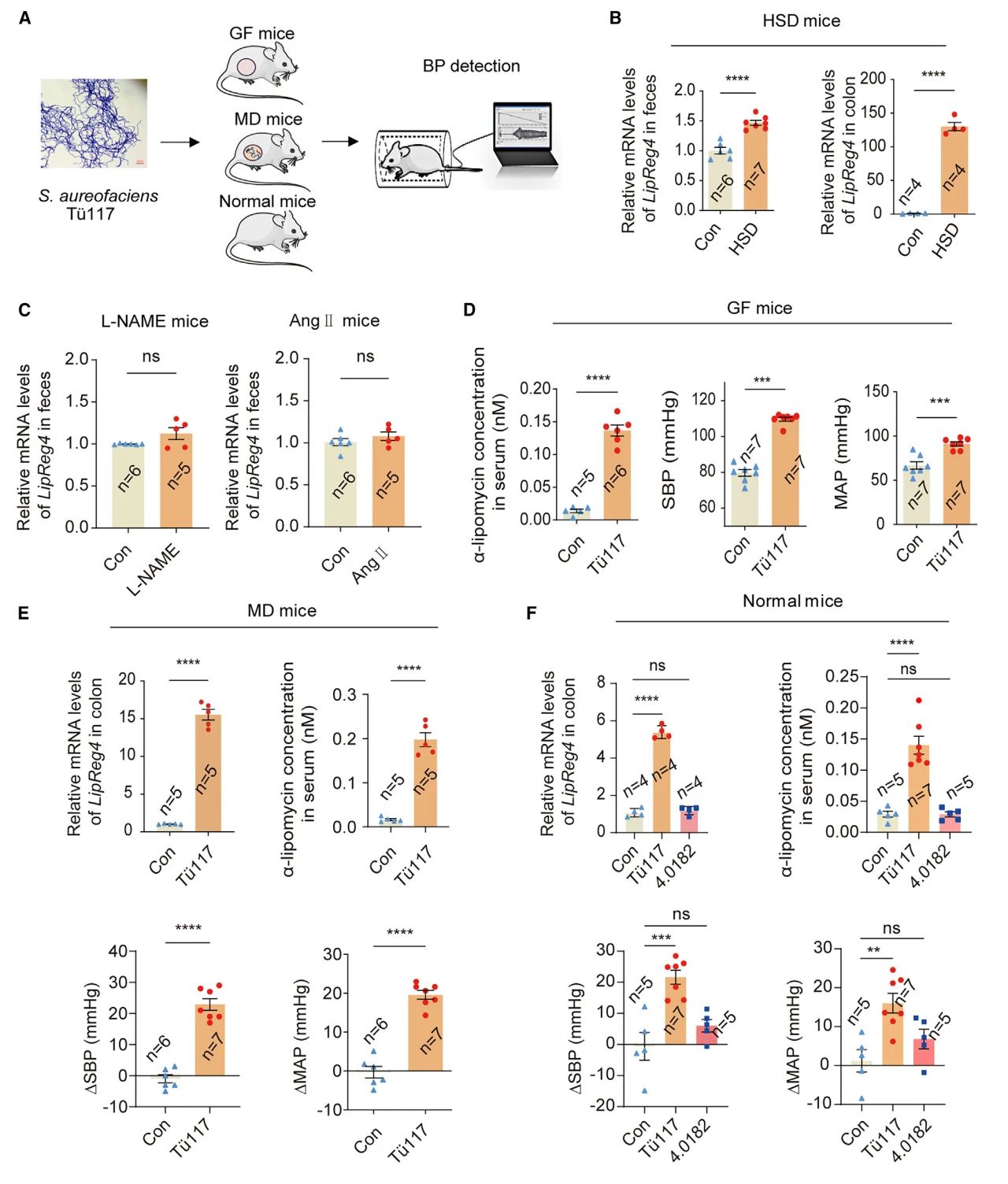 图2 S. aureofaciens Tü117与HSD相关高血压有关
3. 原发性高血压患者的S. aureofaciens Tü117和α-脂霉素水平升高
对已发表的人类公共微生物数据库进行分析,确认了S. aureofaciens Tü117存在于人类粪便样本中。此外作者招募了一个患有原发性高血压的队列,证实LipReg4基因存在于粪便样本中,且LipReg4 mRNA 水平相比对照组显著升高,与Na摄入量成显著相关。
高血压患者血清α-脂霉素含量升高,与Na排泄量显著相关。这些结果证明,S. aureofaciens Tü117和α-脂霉素与原发性高血压患者的Na摄入量有关。
图2 S. aureofaciens Tü117与HSD相关高血压有关
3. 原发性高血压患者的S. aureofaciens Tü117和α-脂霉素水平升高
对已发表的人类公共微生物数据库进行分析,确认了S. aureofaciens Tü117存在于人类粪便样本中。此外作者招募了一个患有原发性高血压的队列,证实LipReg4基因存在于粪便样本中,且LipReg4 mRNA 水平相比对照组显著升高,与Na摄入量成显著相关。
高血压患者血清α-脂霉素含量升高,与Na排泄量显著相关。这些结果证明,S. aureofaciens Tü117和α-脂霉素与原发性高血压患者的Na摄入量有关。
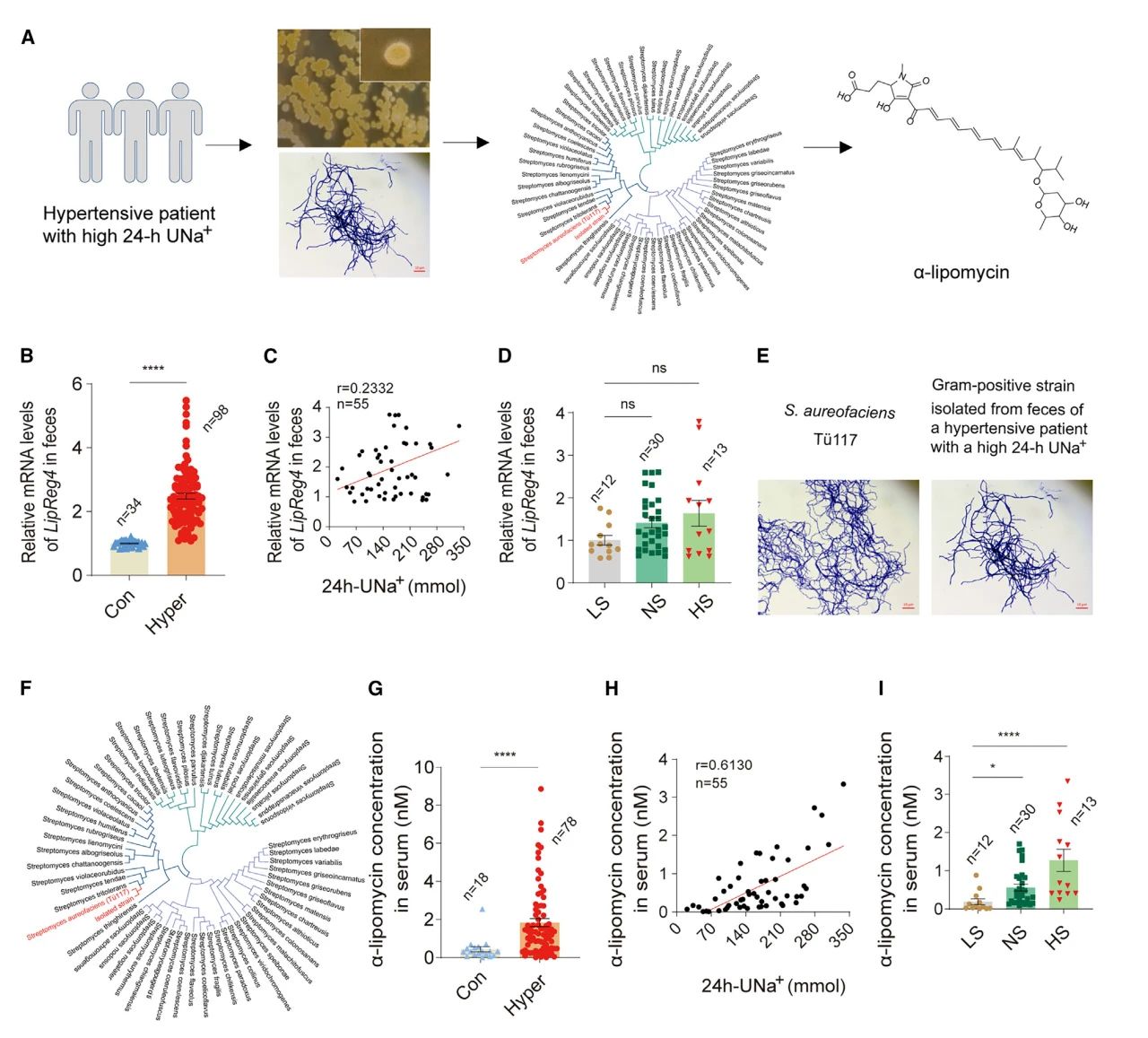 图3 原发性高血压患者的S. aureofaciens Tü117和α-脂霉素水平升高
4. α-脂霉素通过调节内皮TRPV4功能引起血管功能障碍并增加血压
基于分子对接,作者推测钙离子通道蛋白TRPV4可能为α-脂霉素的潜在靶点。细胞功能试验结果表明,α-脂霉素可以显著逆转TRPV4激动剂诱导的细胞内钙离子浓度上升,证明α-脂霉素在体内可作为TRPV4的拮抗剂发挥功能。当α-脂霉素与TRPV4结合时,它会阻断TRPV4通道的活性,抑制钙离子的内流。这导致NO和EDHF途径的激活受阻,血管舒张功能受损,进而引起血管收缩功能增强,最终导致血压升高。
该研究证实,S. aureofaciens Tü117或α-脂霉素处理,均可损害TRPV4激动剂诱导的小鼠血管舒张,但对内皮细胞TRPV4 −/−小鼠无明显影响。这些结果表明,内皮细胞TRPV4通道是S. aureofaciens Tü117调节血压的主要靶点。
图3 原发性高血压患者的S. aureofaciens Tü117和α-脂霉素水平升高
4. α-脂霉素通过调节内皮TRPV4功能引起血管功能障碍并增加血压
基于分子对接,作者推测钙离子通道蛋白TRPV4可能为α-脂霉素的潜在靶点。细胞功能试验结果表明,α-脂霉素可以显著逆转TRPV4激动剂诱导的细胞内钙离子浓度上升,证明α-脂霉素在体内可作为TRPV4的拮抗剂发挥功能。当α-脂霉素与TRPV4结合时,它会阻断TRPV4通道的活性,抑制钙离子的内流。这导致NO和EDHF途径的激活受阻,血管舒张功能受损,进而引起血管收缩功能增强,最终导致血压升高。
该研究证实,S. aureofaciens Tü117或α-脂霉素处理,均可损害TRPV4激动剂诱导的小鼠血管舒张,但对内皮细胞TRPV4 −/−小鼠无明显影响。这些结果表明,内皮细胞TRPV4通道是S. aureofaciens Tü117调节血压的主要靶点。
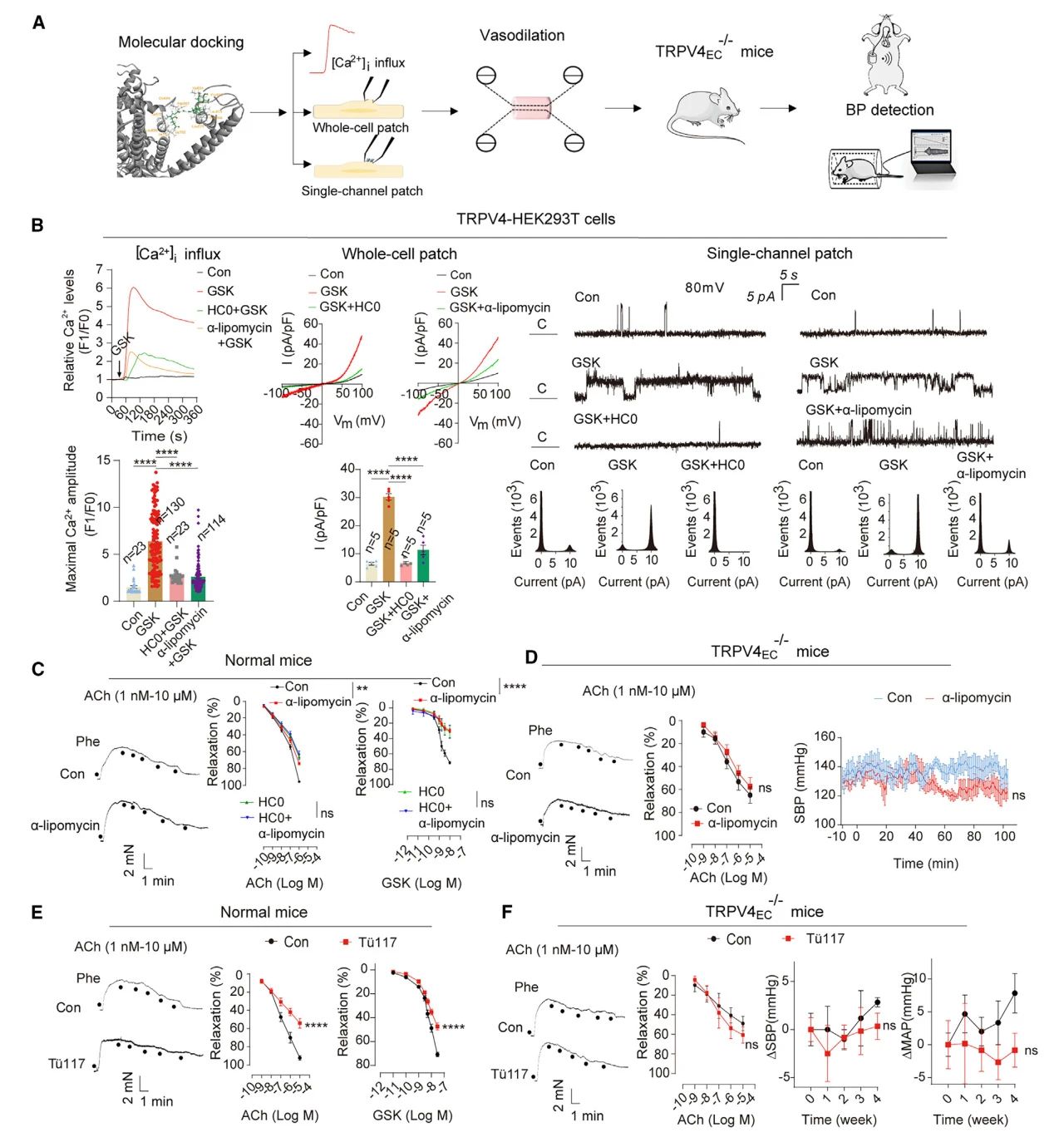 图4 α-脂霉素充当TRPV4拮抗剂
图4 α-脂霉素充当TRPV4拮抗剂
5. 植物乳杆菌CCFM639可改善患者血压 作者测试了多种乳杆菌对S. aureofaciens Tü117的抗菌活性,其中植物乳杆菌CCFM639表现出最强的抗菌作用。CCFM639可改善S. aureofaciens Tü117和HSD诱导的高血压和血管功能障碍,并降低了血液中的α-脂霉素水平和粪便中的LipReg4 mRNA水平。
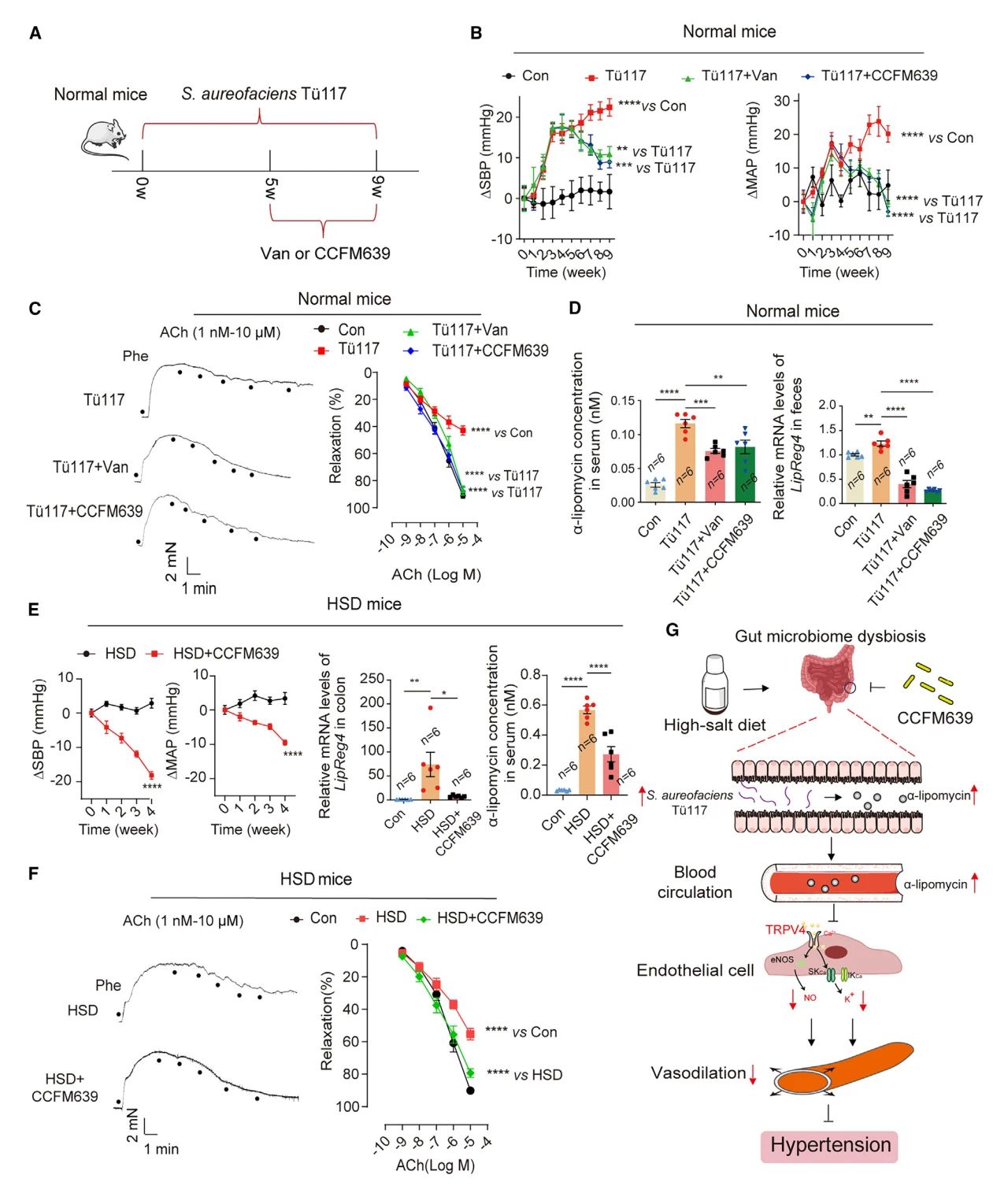 图5 植物乳杆菌CCFM639改善S. aureofaciens Tü117或HSD诱导的血压升高
为了评估CCFM63补充剂对人类血压降低和安全性的影响,作者进行了一项随机安慰剂对照试验。结果显示,为其8周的CCFM63干预显著降低了患者的24小时平均收缩压/舒张压、日渐和夜间收缩压/舒张压,而安慰剂组无明显变化。此外,受试者样本的结果表明,CCFM639的摄入降低了粪便中LipReg4的mRNA水平和血清中的α-脂霉素水平。
图5 植物乳杆菌CCFM639改善S. aureofaciens Tü117或HSD诱导的血压升高
为了评估CCFM63补充剂对人类血压降低和安全性的影响,作者进行了一项随机安慰剂对照试验。结果显示,为其8周的CCFM63干预显著降低了患者的24小时平均收缩压/舒张压、日渐和夜间收缩压/舒张压,而安慰剂组无明显变化。此外,受试者样本的结果表明,CCFM639的摄入降低了粪便中LipReg4的mRNA水平和血清中的α-脂霉素水平。
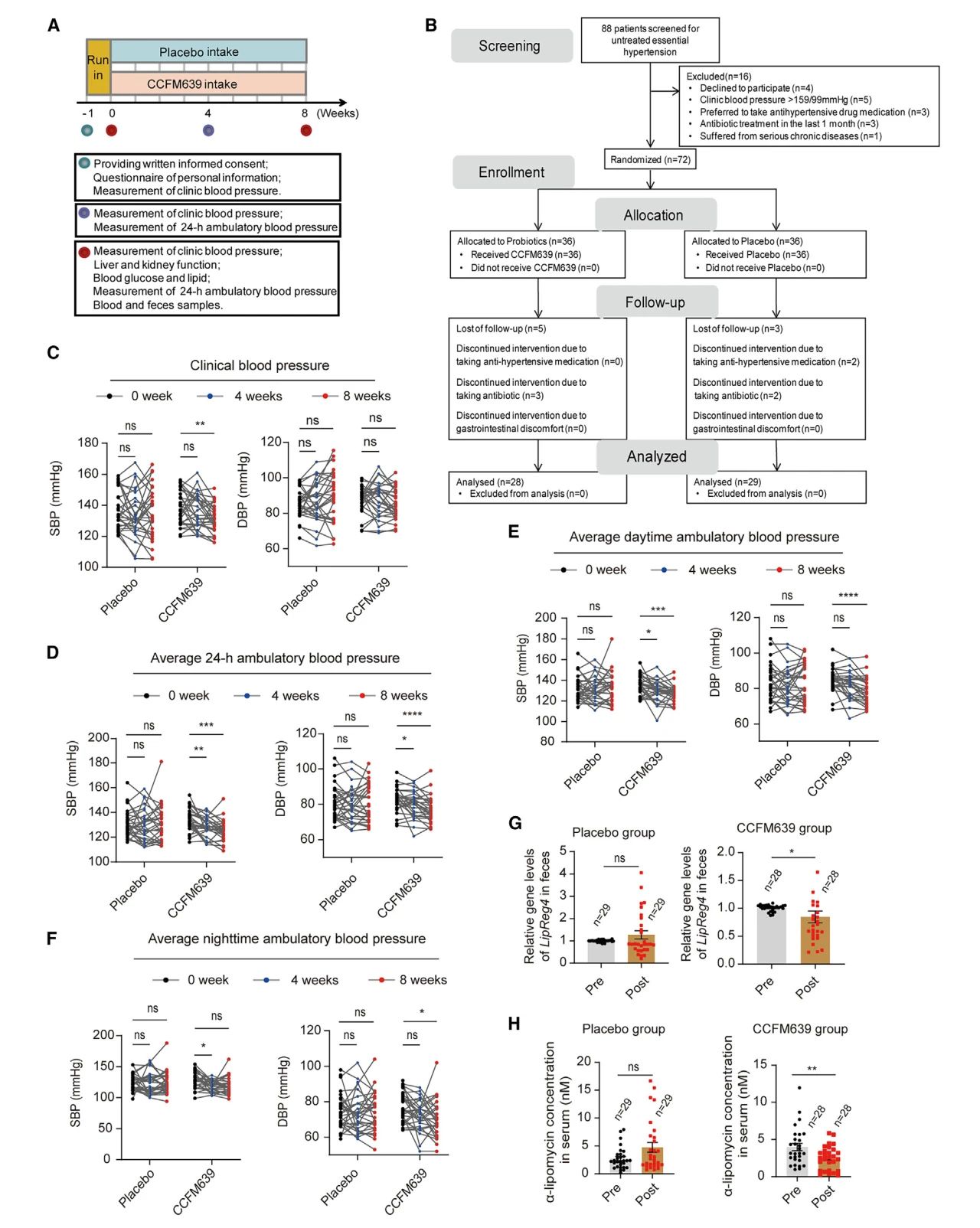 图6 补充CCFM639可降低前期或1期高血压患者的血压
图6 补充CCFM639可降低前期或1期高血压患者的血压
研究小结
该研究表明S. aureofaciens Tü117产生的 α-脂霉素可作为内皮TRPV4拮抗剂,阻断TRPV4的活性并抑制钙离子的内流。这导致NO和EDHF途径的激活受阻,血管舒张功能受损,进而引起血管收缩功能增强,最终导致血压升高。动物试验证明植物乳杆菌CCFM63可改善S. aureofaciens Tü117和HSD诱导的高血压和血管功能障碍。临床试验同样发现了CCFM63对前期或1期高血压且未服用抗高血压药物受试者血压的有益作用。这些结果为预防和治疗轻度高血压提供了新的潜在干预思路。
中科优品推荐 中科新生命自主研发的【G550肠菌高通量靶向代谢组】突破技术瓶颈,采用高通量、高灵敏度平台,可一次性检测近550种肠道菌群相关代谢物,全面、精准反映肠道菌群代谢状态。欢迎感兴趣的老师前来咨询。