上海中科新生命生物科技有限公司
18 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0
- 1
- 0
- 3
文献支持
Label free蛋白质组
询价
公司新闻/正文
J Hazard Mater | 从饮用水到快餐盒,小心这类 “隐形暴露”!中国团队发现PFAS混合暴露让青少年脂肪肝风险飙升
798 人阅读发布时间:2025-07-01 16:19

非酒精性脂肪肝病(NAFLD)已成为全球最常见的慢性肝病,影响着全球超过25%的人口。近年来尤其在青少年中发病率急剧上升,预计到2040年,儿童和青少年患病率将达30.7%。尽管肥胖、胰岛素抵抗和缺乏运动是NAFLD的主要诱因,但环境污染物(特别是某些环境内分泌干扰化学物质)的作用日益受到关注。全氟和多氟烷基物质(PFAS)是一类应用广泛的工业化学品,被归类为“持久性有机污染物”。可通过饮食和水源进入人体,肝脏被认为是PFAS毒性作用的主要靶器官之一。有研究报道PFAS持续在肝脏中积累,会干扰脂质代谢,促进炎症和肝损伤。在青少年中,这种紊乱可能会导致NAFLD的发病以及相关并发症。 2024年12月,上海市疾病预防控制中心化学品毒性检定所体外毒理检测与评价室陶功华、苏州大学公共卫生学院潘臣炜以及复旦大学公共卫生学院郑唯韡团队在 Journal of Hazardous Materials上发表了题为:“Effects of mixed exposure to PFAS on adolescent non-alcoholic fatty liver disease: Integrating evidence from human cohorts, toxicogenomics, and animal models to uncover mechanisms and potential target sites”的研究论文。该研究采用人群研究、毒理基因组学和动物模型的综合方法,探讨PFAS与青少年NAFLD的关联和潜在机制,研究证实PFAS是NAFLD的危险因素,并指出Cyp2e1和Gsta1是预防和治疗PFAS诱导NAFLD的关键靶点。

研究方法 研究对象:在中国西南地区PFAS暴露的代表性地区招募了2014名大理大学新生,其中1694名参与者参与血清暴露物检测。NAFLD的判定根据肝脂肪变性指数(HSI,HSI≥36分被归类为病例组)。最终纳入620例对照(HIS<36)和155例NAFLD患者(HIS≥36)进行后续数据分析。 数据收集:通过标准化问卷调查收集了参与者的社会人口学数据,包括性别、年龄、民族、体重指数(BMI)和吸烟状况。 血清暴露物PFAS测量:使用液相色谱-高分辨率质谱法(LC-HRMS)测量15种PFAS的血清浓度。检测率>40%的PFAS被纳入分析。 统计分析:采用条件logistic回归分析PFAS暴露与NAFLD风险的关系,并使用贝叶斯核机器回归(BKMR)模型和加权分位数和(WQS)回归模型评估PFAS混合物对肝脏功能指标的影响。 毒理基因组学研究:毒理基因组学数据库(CTD)筛选疾病与暴露物相关的基因, GeneMANIA数据库分析基因-基因相互作用网络。进行功能分析,构建PPI网络,筛选关键基因。 动物实验:建立了模拟人类暴露浓度的小鼠模型,通过口服给予不同剂量的PFAS混合物,进行28天的暴露实验,评估其对肝脏的病理学和生化影响。
 图1 研究设计的概览(包括参与者特征、暴露物检测指标以及主要实验步骤)
图1 研究设计的概览(包括参与者特征、暴露物检测指标以及主要实验步骤)
研究结果
1. 全氟和多氟烷基物质暴露与NAFLD风险
以健康人群(HSI<36)作为对照组,NAFLD(HSI≥36)作为病例组,条件logistic回归分析显示两种PFAS(PFHxS和PFOA)暴露与青少年NAFLD风险呈正相关。接着作者采用贝叶斯核机回归模型(BKMR)分析PFAS混合物对青少年NAFLD的影响,模型提示随着PFAS暴露量的增加,先出现抑制作用,随后促进非酒精性脂肪肝病(NAFLD)的趋势。当其他PFAS固定在第25百分位、第50百分位或第75百分位时,NAFLD的风险呈现出单调上升的趋势。单变量暴露-反应关系表明, PFOA、PFDoDA、和PFOS与NAFLD的发生呈正相关(未达到统计学显著),PFHxS与NAFLD的发生呈负相关。在双变量交互作用分析下,发现不同PFAS的影响趋势没有差异,未观察到交互效应。为了评估PFAS的累积效应,使用WQS回归模型评估PFAS混合物对肝脏功能指标的影响。WQS结果显示PFAS暴露与NAFLD之间存在显著的负相关关系,主要由PFHxS驱动。WQS指数还揭示了PFAS暴露与肌酐之间存在显著正相关关系,主要受全戊酸(PFPeA)、全氟己,酸(PFHxA)和全氟脱酰基酸(PFDA)的影响。
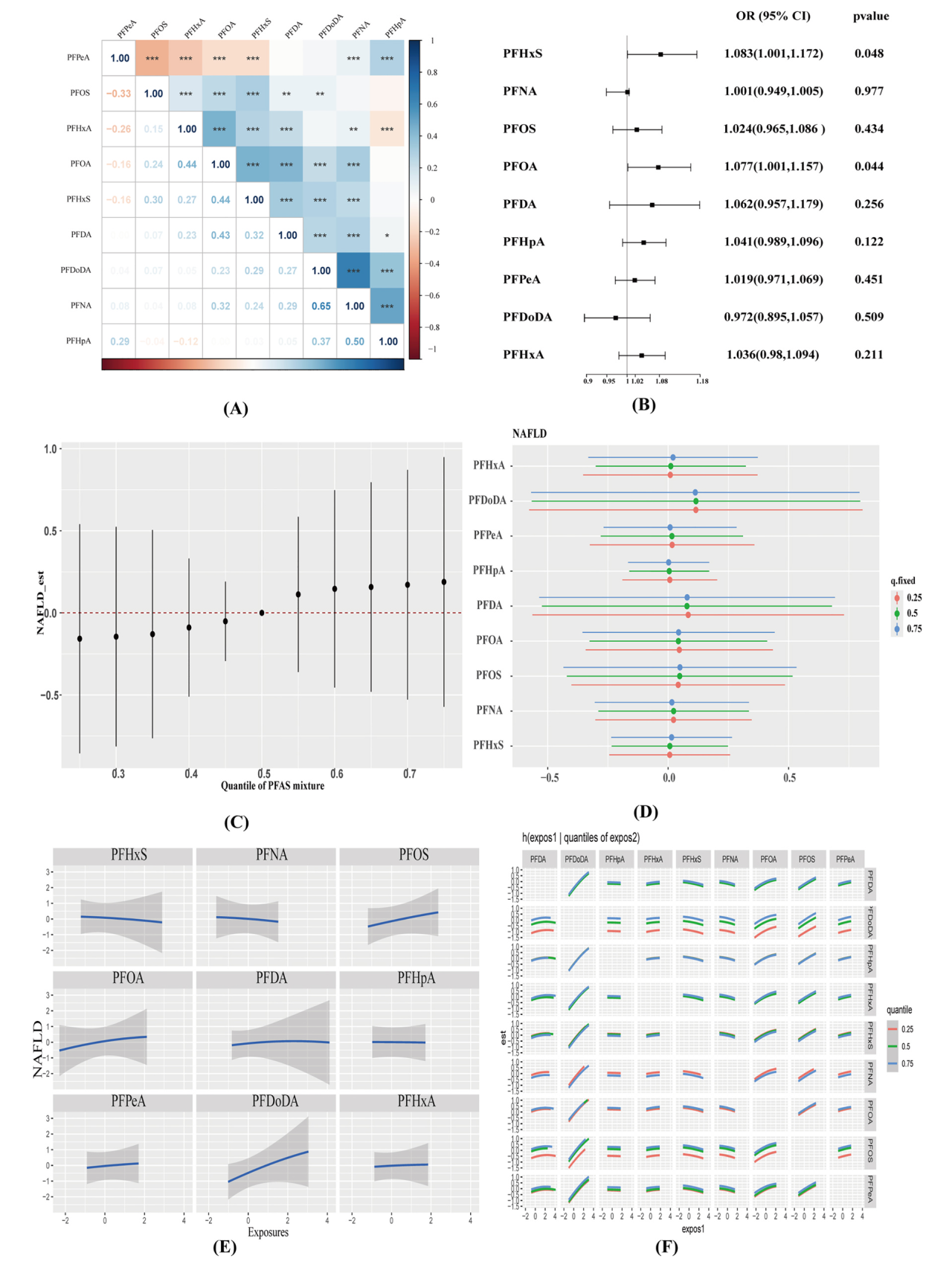 图2 全氟和多氟烷基物质暴露与NAFLD风险
2. 混合PFAS暴露对非酒精性脂肪肝病(NAFLD)的毒理基因组学研究
接下来,作者构建化学-基因-表型-疾病网络。通过在CTD数据库中筛选,识别出NAFLD与PFAS相关的78个常见基因,并使用GeneMANIA进一步探索这些基因之间的相互作用。作者对这些关键基因进行了GO和KEGG分析,以识别它们的潜在功能。GO分析显示,负调控间隙连接组装、谷胱甘肽衍生物生物合成等分子功能显著富集,提示PFAS可能干扰细胞连接调控、氧化应激响应及内分泌调节; KEGG分析则表明,酒精性肝病、癌症通路、非酒精性脂肪肝病、脂质代谢及药物代谢-细胞色素P450等通路与PFAS诱导的NAFLD密切相关。接下来,作者构建了一个PPI网络来探索探索PFAS诱导NAFLD的核心靶点蛋白。其中大部分与各种肝脏代谢酶有关。例如参与乙醇代谢的酒精脱氢酶家族(ADH)、催化乙,醛氧化的乙,醛脱氢酶(ALDH)、调控氧化应激与解毒过程的谷胱甘肽S-转移酶(GST)以及细胞色素P450(CYP2E1)。这些肝脏代谢酶的功能改变可能会加剧氧化应激和脂肪变性,进而参与NAFLD的发生发展。
图2 全氟和多氟烷基物质暴露与NAFLD风险
2. 混合PFAS暴露对非酒精性脂肪肝病(NAFLD)的毒理基因组学研究
接下来,作者构建化学-基因-表型-疾病网络。通过在CTD数据库中筛选,识别出NAFLD与PFAS相关的78个常见基因,并使用GeneMANIA进一步探索这些基因之间的相互作用。作者对这些关键基因进行了GO和KEGG分析,以识别它们的潜在功能。GO分析显示,负调控间隙连接组装、谷胱甘肽衍生物生物合成等分子功能显著富集,提示PFAS可能干扰细胞连接调控、氧化应激响应及内分泌调节; KEGG分析则表明,酒精性肝病、癌症通路、非酒精性脂肪肝病、脂质代谢及药物代谢-细胞色素P450等通路与PFAS诱导的NAFLD密切相关。接下来,作者构建了一个PPI网络来探索探索PFAS诱导NAFLD的核心靶点蛋白。其中大部分与各种肝脏代谢酶有关。例如参与乙醇代谢的酒精脱氢酶家族(ADH)、催化乙,醛氧化的乙,醛脱氢酶(ALDH)、调控氧化应激与解毒过程的谷胱甘肽S-转移酶(GST)以及细胞色素P450(CYP2E1)。这些肝脏代谢酶的功能改变可能会加剧氧化应激和脂肪变性,进而参与NAFLD的发生发展。
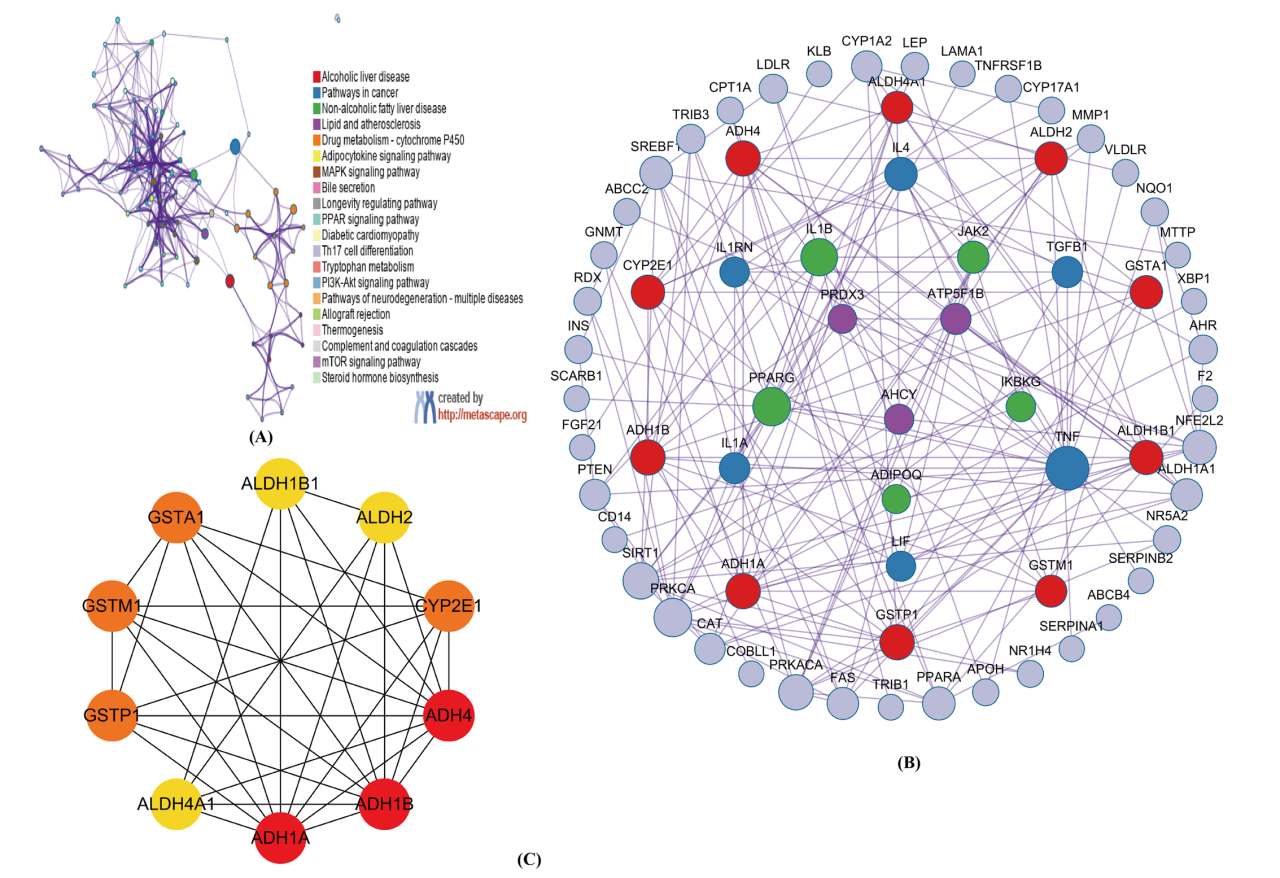 图3 混合PFAS暴露对非酒精性脂肪肝病(NAFLD)的毒理基因组学研究
3. PFAS暴露:体内实验验证结果
利用动物实验模拟了青少年暴露条件,进一步观察PFAS暴露对肝脏靶器官产生的影响。组织病理学提示,随着PFAS处理浓度增加,肝脏超微结构发生显著变化,从细胞间质、细胞器的损伤,脂滴累积,到炎症浸润、细胞坏死、纤维化等病变逐渐加重。说明PFAS对肝脏具有明显的剂量依赖性毒性作用,且该毒性作用涉及细胞器功能障碍、炎症反应及纤维化等多个方面。肝功能生物标志物谷草转氨酶(AST)、谷丙转氨酶(ALT)、总胆红素(TBIL)、直接胆红素和肌酐(CREA)水平均异常。以上结果说明PFAS处理后会引起肝脏损伤、肝脏胆汁淤积和胆管阻塞。
图3 混合PFAS暴露对非酒精性脂肪肝病(NAFLD)的毒理基因组学研究
3. PFAS暴露:体内实验验证结果
利用动物实验模拟了青少年暴露条件,进一步观察PFAS暴露对肝脏靶器官产生的影响。组织病理学提示,随着PFAS处理浓度增加,肝脏超微结构发生显著变化,从细胞间质、细胞器的损伤,脂滴累积,到炎症浸润、细胞坏死、纤维化等病变逐渐加重。说明PFAS对肝脏具有明显的剂量依赖性毒性作用,且该毒性作用涉及细胞器功能障碍、炎症反应及纤维化等多个方面。肝功能生物标志物谷草转氨酶(AST)、谷丙转氨酶(ALT)、总胆红素(TBIL)、直接胆红素和肌酐(CREA)水平均异常。以上结果说明PFAS处理后会引起肝脏损伤、肝脏胆汁淤积和胆管阻塞。
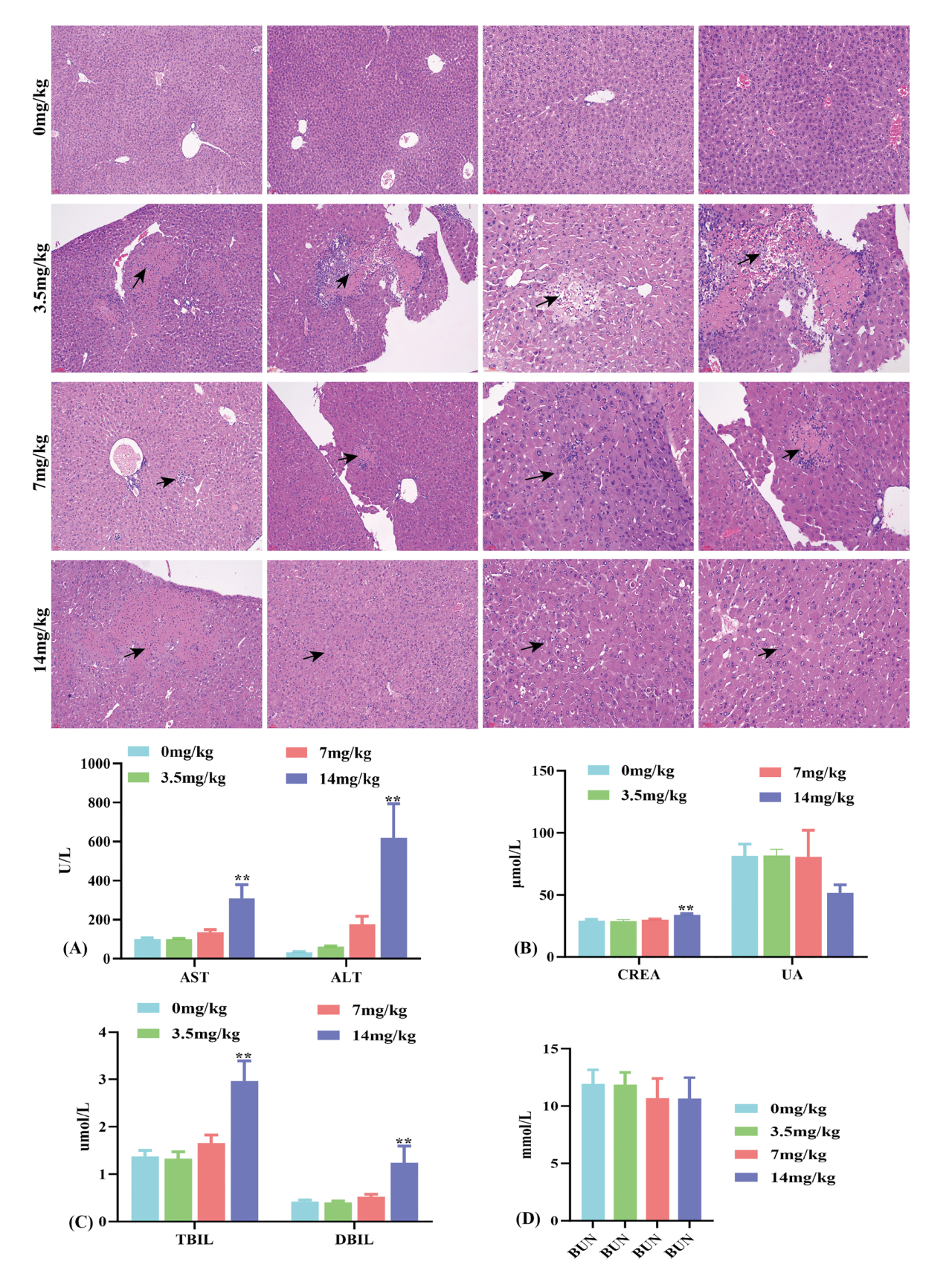 图4 动物模型验证PFAS混合暴露对肝脏的病理影响
4.毒理基因组学结果验证
以定量PCR分析八种与NAFLD相关的核心基因。与对照组相比,与肝脏代谢相关的关键基因表达发生变化,包括Aldh4a1、Adh4、Cyp2e1、Gsta1。在PFAS暴露下,Cyp2e1和Gsta1的表达呈钟形曲线,有助于清除环境污染物代谢产物。结果提示,细胞色素P450同工酶(Cyp2e1),其因PFAS暴露而增加的活性加剧氧化应激和脂质过氧化,导致肝细胞损伤。因此,后续可进一步探索CYP2E1抑制剂(如氯唑沙宗)减轻PFAS诱导的肝毒性的潜在应用价值。谷胱甘肽S-转移酶1(Gsta1)的上调可以缓解油酸或高脂饮食诱导的肝脂肪变性,并且通过与脂肪酸结合蛋白1(FABP1)相互作用,抑制细胞内甘油三酯的合成,也具有未来药物开发靶点的潜力。
图4 动物模型验证PFAS混合暴露对肝脏的病理影响
4.毒理基因组学结果验证
以定量PCR分析八种与NAFLD相关的核心基因。与对照组相比,与肝脏代谢相关的关键基因表达发生变化,包括Aldh4a1、Adh4、Cyp2e1、Gsta1。在PFAS暴露下,Cyp2e1和Gsta1的表达呈钟形曲线,有助于清除环境污染物代谢产物。结果提示,细胞色素P450同工酶(Cyp2e1),其因PFAS暴露而增加的活性加剧氧化应激和脂质过氧化,导致肝细胞损伤。因此,后续可进一步探索CYP2E1抑制剂(如氯唑沙宗)减轻PFAS诱导的肝毒性的潜在应用价值。谷胱甘肽S-转移酶1(Gsta1)的上调可以缓解油酸或高脂饮食诱导的肝脂肪变性,并且通过与脂肪酸结合蛋白1(FABP1)相互作用,抑制细胞内甘油三酯的合成,也具有未来药物开发靶点的潜力。
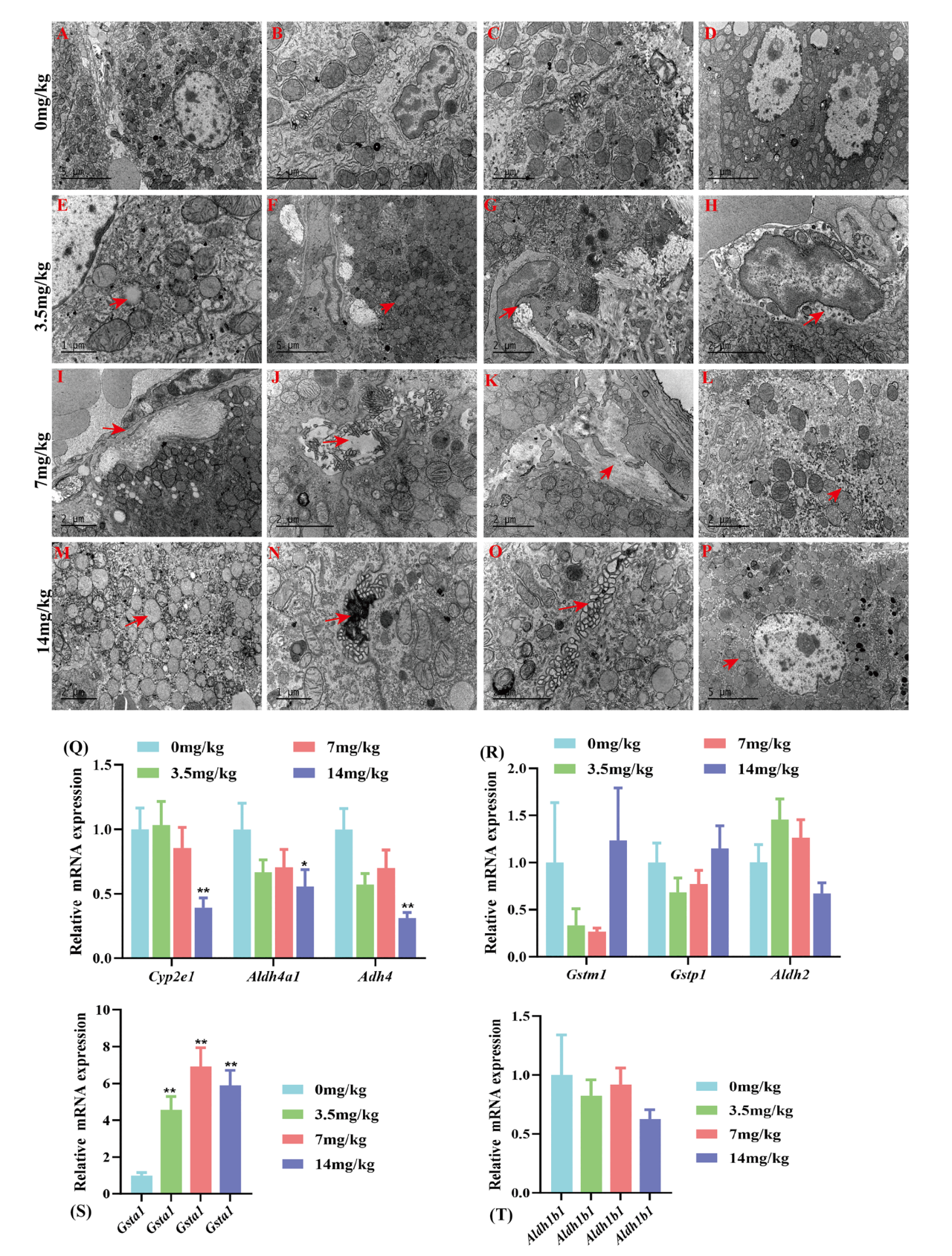 图5 毒理基因组学结果验证
图5 毒理基因组学结果验证
健康生活小妙招
PFAS进入人体主要有三种途径:一是吃进来,二是吸进来,三是皮肤接触。
在饮食方面:注意减少购买使用防油包装纸包装的快餐、糕点等,优先选择玻璃容器或纸质包装的食品;注意避免食用受污染水域的鱼类,因为PFAS易在水体及生物体内蓄积。
在生活用品方面:可以用铸铁锅等替代含有PFAS的不粘锅;挑选不含PFAS的防水、防污织物产品。
在日常习惯方面:尽量少用含PFAS的一次性纸制品,比如一些防水纸杯等;关注饮用水水源情况,有条件可使用能有效过滤PFAS的净水器,确保饮水安全。
中科优品推荐 【中科新生命】针对暴露组学研究,特提供高端定制方案,除全面的暴露组检测产品外,配套微生物组、代谢组等多组学检测服务与完善的生信分析服务,针对暴露组对人群队列健康影响提供一站式研究解决方案,为您的研究精准定位,保驾护航。欢迎感兴趣的老师前来咨询!