上海中科新生命生物科技有限公司
18 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0
- 1
- 0
- 3
文献支持
空间多组学
询价
公司新闻/正文
Cancer Cell (IF 50.3)| 空间多组学揭示胶质母细胞瘤中双向肿瘤-宿主相互依赖性
456 人阅读发布时间:2023-09-06 11:01
尽管单细胞技术为恶性肿瘤中单个细胞的转录调节和动态进化提供了见解, 但由于空间组织信息的丢失,单细胞分析只能提供细胞相互作用的间接推断。在大脑中,空间组织和功能密切相关。因此,在空间分辨的背景下全面研究由于微环境而导致的胶质瘤的各种转录适应极具必要性。
2022年6月,来自德国弗赖堡大学的研究团队在Cancer Cell(IF 50.3)杂志上发表题为“Spatially resolved multi-omics deciphers bidirectional tumor-host interdependence in glioblastoma”的研究文章,该研究揭示了胶质母细胞瘤的空间生态位受到肿瘤微环境的影响,对炎症或代谢刺激产生转录适应,并概括了不同的神经发育阶段。

研究材料
脑胶质瘤患者肿瘤组织冰冻切片;不同年龄段人、大鼠皮质区切片诱导的皮质类器官
技术路线
脑胶质瘤患者肿瘤组织冰冻切片;不同年龄段人、大鼠皮质区切片诱导的皮质类器官
技术路线
步骤1:绘制胶质母细胞瘤的空间水平转录图谱;
步骤2:探究由空间决定的转录异质性;
步骤3:空间上不同的转录程序与亚克隆结构;
步骤4:联合空间代谢组揭示GBM中与反应性缺氧相关的代谢改变;
步骤5:TCGA和缺氧相关CNA改变的细胞培养验证;
步骤6:建立缺氧应激概念以及逃逸机制的说明;
步骤7:肿瘤-宿主在反应性免疫区域相互依赖的探索;
步骤8:体外皮层培养显示了环境影响的双向转移。
研究结果
1. 绘制胶质母细胞瘤的空间水平转录图谱
作者对来自20位患者的28个胶质瘤样本进行空间转录组学测序,得到了不同年龄组和不同解剖区域的88,793个Spot为单位的转录组数据。此外,作者还对同类型的组织切片进行了空间代谢组学(n=6)和蛋白质组学检测(n=14),来从多组学角度综合探究GBM的空间生物信息变化。在基于相互最近邻(MNN)的水平整合和共享最近邻域(SNN)的聚类后,观察到非恶性的组织特性在患者之间表现为相似的,而恶性细胞的表达在患者间存在明显的异质性。
随后,利用基于机器学习的分割技术与人工神经网络(ANN)模型,对空间转录组数据使用了去卷积的处理,在所有样本的88,793个Spot中,观察到63,121个Spot来自恶性细胞,其中46,459个Spot包含至少95%的肿瘤细胞。根据组织学分类系统预测了每个Spot的组织学表型,发现肿瘤细胞占比低的样本主要是因为包含浸润区域而导致的。
步骤2:探究由空间决定的转录异质性;
步骤3:空间上不同的转录程序与亚克隆结构;
步骤4:联合空间代谢组揭示GBM中与反应性缺氧相关的代谢改变;
步骤5:TCGA和缺氧相关CNA改变的细胞培养验证;
步骤6:建立缺氧应激概念以及逃逸机制的说明;
步骤7:肿瘤-宿主在反应性免疫区域相互依赖的探索;
步骤8:体外皮层培养显示了环境影响的双向转移。
研究结果
1. 绘制胶质母细胞瘤的空间水平转录图谱
作者对来自20位患者的28个胶质瘤样本进行空间转录组学测序,得到了不同年龄组和不同解剖区域的88,793个Spot为单位的转录组数据。此外,作者还对同类型的组织切片进行了空间代谢组学(n=6)和蛋白质组学检测(n=14),来从多组学角度综合探究GBM的空间生物信息变化。在基于相互最近邻(MNN)的水平整合和共享最近邻域(SNN)的聚类后,观察到非恶性的组织特性在患者之间表现为相似的,而恶性细胞的表达在患者间存在明显的异质性。
随后,利用基于机器学习的分割技术与人工神经网络(ANN)模型,对空间转录组数据使用了去卷积的处理,在所有样本的88,793个Spot中,观察到63,121个Spot来自恶性细胞,其中46,459个Spot包含至少95%的肿瘤细胞。根据组织学分类系统预测了每个Spot的组织学表型,发现肿瘤细胞占比低的样本主要是因为包含浸润区域而导致的。
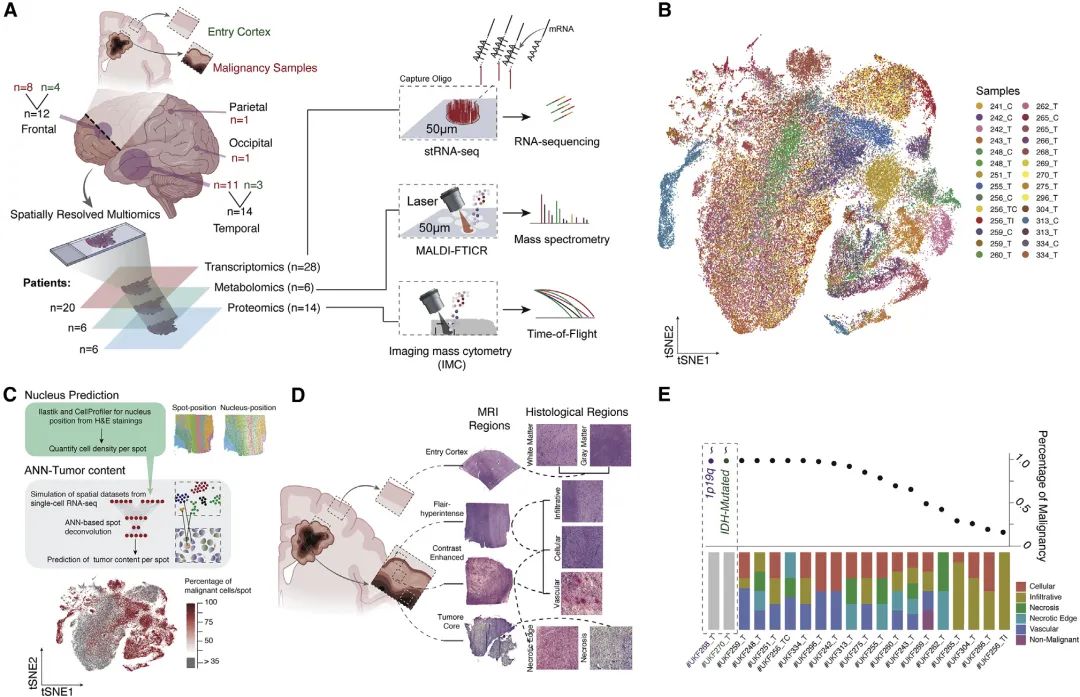
图1 整体研究思路与胶质母细胞瘤空间转录图谱
2. 探究由空间决定的转录异质性
作者根据不同的转录特征和细胞周期模块对所有Spot进行了分类,发现被分类为神经元发育和反应性缺氧相关的Spot在定义为周期细胞中被检测的丰度较低,其他转录模块则较平均的分布于所有细胞周期状态。再进一步将目前几个公开的Bulk RNA-seq、scRNA-seq数据集与该研究中的stRNA-seq进行了空间加权回归整合,证实与神经胶质相关的程序放射状胶质、空间OPC和神经元发育分别与AC-,OPC-和NPC-like有着较强的重叠。
作者发现,反应性免疫程序与“混合”细胞群的关联性是在空间上所独有的,这些“混合”细胞群跨越AC和MES-like状态,或与包含AC和MES-like状态的细胞相靠近。此外,作者还分析了组织学和空间转录集群之间的空间一致性,发现在组织学坏死区域周围,反应性缺氧程序显著富集。
拷贝数改变(CNAs,包括癌基因的局灶性扩增或肿瘤抑制因子的缺失)是恶性细胞的标志, CNAs的改变可驱动治疗耐药和肿瘤复发。作者利用推断的CNAs事件研究了基因组改变和空间上不同的转录程序之间的关系,发现在反应性缺氧相关的Spot中出现了作为独立的亚克隆事件CNAs的显著积累。
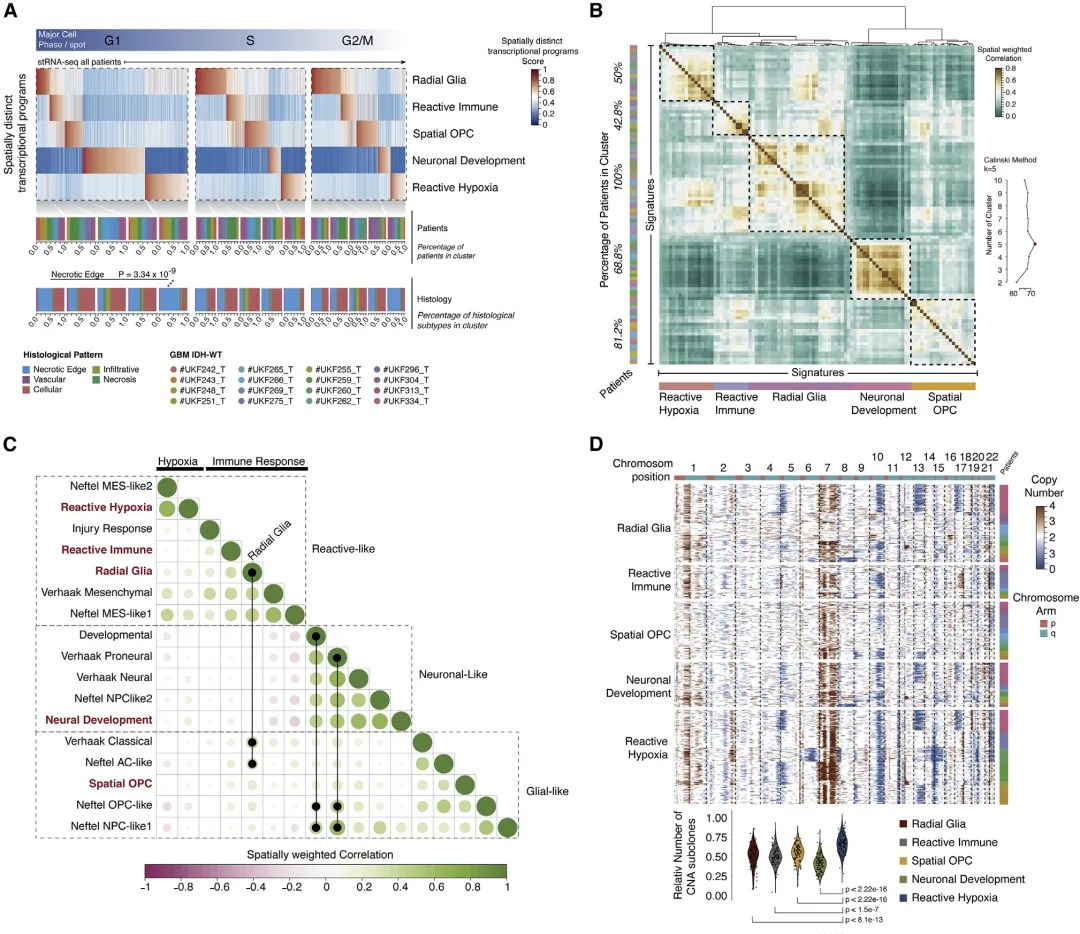
图2 由空间决定的转录异质性
3. 空间上不同的转录程序和亚克隆结构
为了探究空间上的转录多样性是否可以直接反映肿瘤内的遗传亚克隆,作者通过患者特异性CNAs的层次聚类重建了克隆结构,并确定了每个亚克隆内个体间和空间上不同转录模块的分布,在26.32%的亚克隆中,单一转录程序占主导地位(每个亚克隆的Spot超过75%)。这说明,克隆结构对空间上不同的转录程序的发生没有显著影响,但亚克隆也会偶尔偏好于空间OPC(8.77%)或反应性缺氧程序(10.52%)。
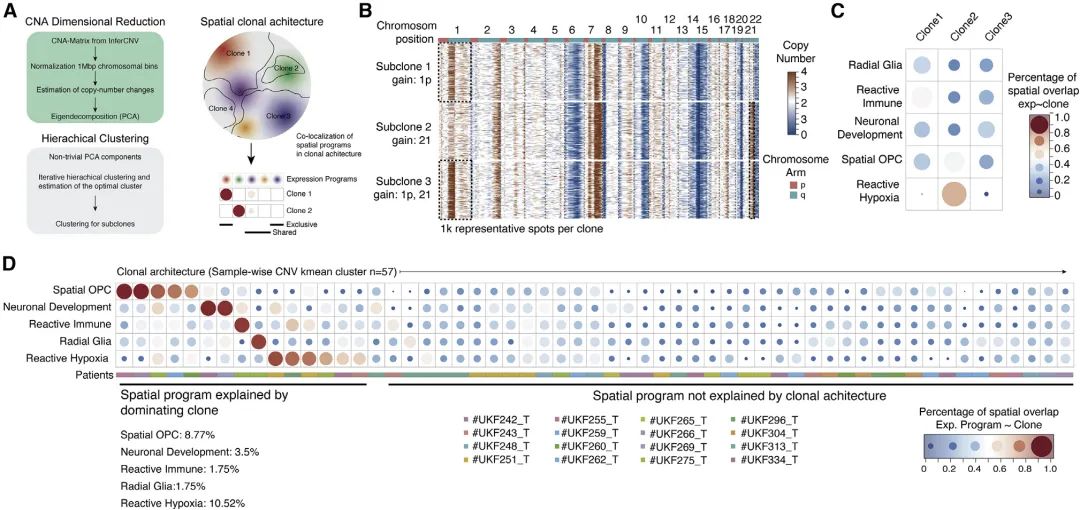
图3 空间上不同的转录程序和亚克隆结构
4. GBM中与反应性缺氧相关的代谢改变
将空间代谢组数据与stRNA-seq数据的整合分析,识别出三个显著的代谢亚组。功能代谢分析显示,磷酸戊糖通路在第一个代谢模块(M-G1)中显著富集, M-G2的特征是磷酸腺苷代谢的富集,这也是胶质瘤代谢的标志; M-G3在糖酵解和氨基糖代谢方面显著富集。
通过WNN聚类发现数据中反应性低氧的空间转录组模块作为一个独特的集群出现,被分配到反应性缺氧通路的大多数Spot位于坏死组织的边缘。作者联系之前观察到的空间CNAs分布分析结果,认为低氧代谢导致基因组不稳定性会在空间分离的生态位中积累,代表了新发生的基因组改变的潜在来源,而且这些改变可能利于肿瘤细胞产生治疗耐药性。
将空间代谢组数据与stRNA-seq数据的整合分析,识别出三个显著的代谢亚组。功能代谢分析显示,磷酸戊糖通路在第一个代谢模块(M-G1)中显著富集, M-G2的特征是磷酸腺苷代谢的富集,这也是胶质瘤代谢的标志; M-G3在糖酵解和氨基糖代谢方面显著富集。
通过WNN聚类发现数据中反应性低氧的空间转录组模块作为一个独特的集群出现,被分配到反应性缺氧通路的大多数Spot位于坏死组织的边缘。作者联系之前观察到的空间CNAs分布分析结果,认为低氧代谢导致基因组不稳定性会在空间分离的生态位中积累,代表了新发生的基因组改变的潜在来源,而且这些改变可能利于肿瘤细胞产生治疗耐药性。

图4 整合空间代谢组与空间转录组的数据
5. TCGA和缺氧相关CNA改变的细胞培养验证
为了进一步验证以上发现,作者分析了来自TCGA数据库的样本(IDH1/2基因型GBM患者,n=357),并根据缺氧基因表达评分对患者进行了分类。缺氧驱动的肿瘤显示了染色体改变的显著增加,这证实了前文的观察结果,并进一步证实了代谢和基因组不稳定性之间的关系。为了该假设,在常氧和低氧条件下培养了原代胶质母细胞瘤细胞系2-6周(n=4)。拷贝数变异揭示了CNA谱的差异,慢性缺氧条件下CNA事件的显著累积证实了应激诱导CNA改变的假设。
为了进一步验证以上发现,作者分析了来自TCGA数据库的样本(IDH1/2基因型GBM患者,n=357),并根据缺氧基因表达评分对患者进行了分类。缺氧驱动的肿瘤显示了染色体改变的显著增加,这证实了前文的观察结果,并进一步证实了代谢和基因组不稳定性之间的关系。为了该假设,在常氧和低氧条件下培养了原代胶质母细胞瘤细胞系2-6周(n=4)。拷贝数变异揭示了CNA谱的差异,慢性缺氧条件下CNA事件的显著累积证实了应激诱导CNA改变的假设。
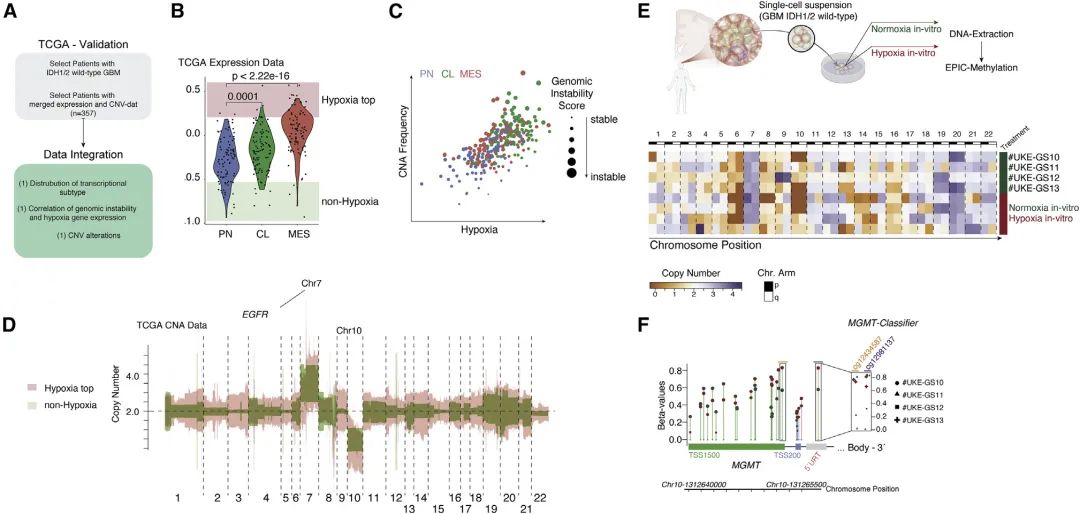
图5 TCGA和缺氧相关CNA改变的细胞培养验证
6. 缺氧应激概念和逃逸机制的说明
研究观察到特别是S期阻滞在缺氧核心点中很明显,因此作者又进一步提出了以下假设:缺氧导致的S期阻滞导致了基因组不稳定性的积累,即应激反应和有丝分裂检查点的改变导致了细胞非整倍体性。作者估算出空间基因表达轨迹的目的,从而能够识别空间上相反的转录通路,发现缺氧反应和迁移特征显示出反向的空间轨迹。综上所述,作者的研究结果表明,代谢变化和氧化应激是基因组多样性的潜在相互驱动因素,从而导致GBM的克隆进化。
研究观察到特别是S期阻滞在缺氧核心点中很明显,因此作者又进一步提出了以下假设:缺氧导致的S期阻滞导致了基因组不稳定性的积累,即应激反应和有丝分裂检查点的改变导致了细胞非整倍体性。作者估算出空间基因表达轨迹的目的,从而能够识别空间上相反的转录通路,发现缺氧反应和迁移特征显示出反向的空间轨迹。综上所述,作者的研究结果表明,代谢变化和氧化应激是基因组多样性的潜在相互驱动因素,从而导致GBM的克隆进化。
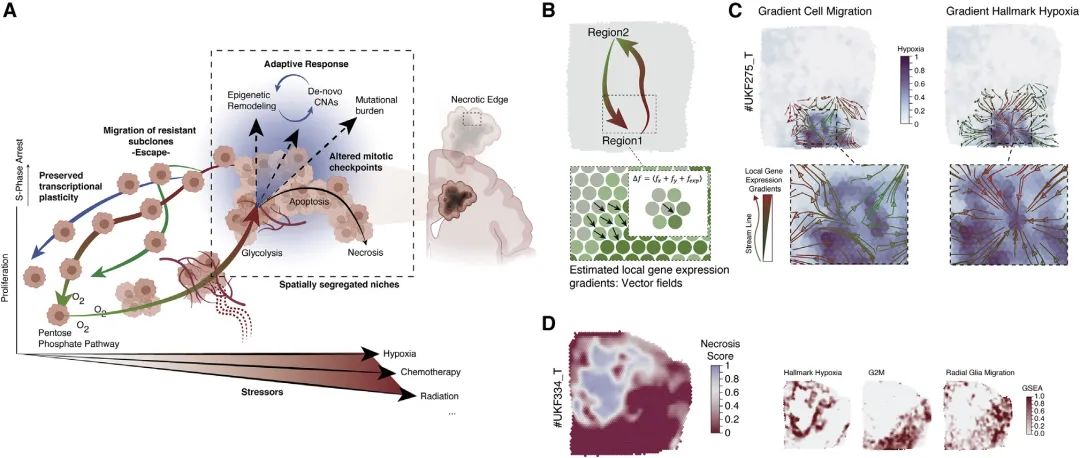
图6 缺氧应激概念和逃逸机制的说明
7. 肿瘤-宿主在反应性免疫区域相互依赖的探索
对于空间蛋白质组,在反应性免疫和反应性缺氧程序的区域内选择ROI(感兴趣的区域),并从分类为神经元分化的区域中选择空白对照ROI (n=6例患者,14个不同的1,000 μm2 ROI),在分割后获得了一个包含82,179个细胞的全面蛋白质组学图谱。作者通过将细胞细分为放射状胶质(EGFR+HOPX+),反应性免疫(EGFR+CHI3L1+VIM+),空间OPC(EGFR+OLIG1+),神经发育(EGFR+SNAP25+-CALM2+)和反应性缺氧(EGFR+VEGFA+)来量化细胞多样性。反应性免疫(EGFR+CHI3L1+VIM+)细胞仅在转录定义的反应性免疫定位中得到证实。
为了补充关于免疫系统和GBM之间的细胞关系,作者建立了细胞相互依赖模型,根据肿瘤细胞与淋巴样或髓样细胞的距离量化了它们之间的细胞连接,以此来证实在反应性免疫区域中,肿瘤细胞与免疫区域之间的细胞相互作用存在着增强。
对于空间蛋白质组,在反应性免疫和反应性缺氧程序的区域内选择ROI(感兴趣的区域),并从分类为神经元分化的区域中选择空白对照ROI (n=6例患者,14个不同的1,000 μm2 ROI),在分割后获得了一个包含82,179个细胞的全面蛋白质组学图谱。作者通过将细胞细分为放射状胶质(EGFR+HOPX+),反应性免疫(EGFR+CHI3L1+VIM+),空间OPC(EGFR+OLIG1+),神经发育(EGFR+SNAP25+-CALM2+)和反应性缺氧(EGFR+VEGFA+)来量化细胞多样性。反应性免疫(EGFR+CHI3L1+VIM+)细胞仅在转录定义的反应性免疫定位中得到证实。
为了补充关于免疫系统和GBM之间的细胞关系,作者建立了细胞相互依赖模型,根据肿瘤细胞与淋巴样或髓样细胞的距离量化了它们之间的细胞连接,以此来证实在反应性免疫区域中,肿瘤细胞与免疫区域之间的细胞相互作用存在着增强。

图7 肿瘤-宿主在反应性免疫区域相互依赖的探索
8. 体外皮层培养显示了环境影响的双向转移
为了评估各种微环境的影响,作者采集了来自多个不同年龄患者的脑皮质组织(2-85岁,患者n=3;切片n=48,每个患者16个)以及2周和2岁大鼠的供体(n=32个)切片。观察到发育状态相关的表达特征(OPC-,AC-和NPC-like)在人供体组织培养中的细胞中过表达,而且主要出现在青年和中年供体中(2/3)。在啮齿类动物神经环境中培养的GBM细胞富集了MES-1/2和AC-like转录特征。发育状态的周期细胞仅在OPC-like亚群中检测到。RNA Velocity显示,从体外细胞培养初始状态到类似MES和AC的末段状态的预计向量方向代表了细胞变化由神经环境而驱动并产生定向适应。蛋白酪氨酸磷酸酶受体Z1型(PTPRZ1)作为胶质细胞径向分化的常见标志基因,在MES-AC杂合状态下的细胞轨迹中被分配为高度参与了这一细胞状态转变。该数据证实了在OPC-和NPC-like分支中的双向命运。编码钾离子通道(KCNH8)和代谢型谷氨酸受体(GRM3)的基因也在这些转录模块中表现出高度参与了该细胞状态的转变,表明神经元环境促进了特定的转录偏好转变,也与目前关于神经元-胶质瘤相互作用的研究报道一致。
为了评估各种微环境的影响,作者采集了来自多个不同年龄患者的脑皮质组织(2-85岁,患者n=3;切片n=48,每个患者16个)以及2周和2岁大鼠的供体(n=32个)切片。观察到发育状态相关的表达特征(OPC-,AC-和NPC-like)在人供体组织培养中的细胞中过表达,而且主要出现在青年和中年供体中(2/3)。在啮齿类动物神经环境中培养的GBM细胞富集了MES-1/2和AC-like转录特征。发育状态的周期细胞仅在OPC-like亚群中检测到。RNA Velocity显示,从体外细胞培养初始状态到类似MES和AC的末段状态的预计向量方向代表了细胞变化由神经环境而驱动并产生定向适应。蛋白酪氨酸磷酸酶受体Z1型(PTPRZ1)作为胶质细胞径向分化的常见标志基因,在MES-AC杂合状态下的细胞轨迹中被分配为高度参与了这一细胞状态转变。该数据证实了在OPC-和NPC-like分支中的双向命运。编码钾离子通道(KCNH8)和代谢型谷氨酸受体(GRM3)的基因也在这些转录模块中表现出高度参与了该细胞状态的转变,表明神经元环境促进了特定的转录偏好转变,也与目前关于神经元-胶质瘤相互作用的研究报道一致。

图8 体外人类皮层培养显示了环境影响的双向转移
小编小结
在过去的几年中,通过单细胞分析技术的进步所取得的许多发现彻底改变了人们对肿瘤异质性和可塑性,以及潜在治疗方案的理解。然而,脑肿瘤内空间组织的生物学意义尚不清楚。该研究阐明了GBM的空间转录模式图谱,并绘制了包括代谢和肿瘤-宿主细胞相互作用的微环境景观,揭示了微环境和GBM转录异质性的时空变化之间的双向和单向相互作用。